65岁的老张和同龄的老李,看起来年纪相仿,活法却差得远。老张每天晨练、买菜、带孙子;老李走路不稳,动不动就累,小毛病也没断过。医学上把这种"生理储备下降、应对压力能力减弱"的状态称为"衰弱"——不是老了,而是身体各系统协调出了问题。
浙江大学等团队发表在《Cell Metabolism》的研究,分析了50,506名参与者的2,911种血浆蛋白,是目前规模最大的衰弱蛋白质组学研究。研究最终锁定了1,339种与衰弱显著相关的蛋白,其中90%在衰弱程度加重时水平升高。这让人倾向于一个解释:衰弱不是某几个指标出问题,而是蛋白质紊乱持续累积的过程。
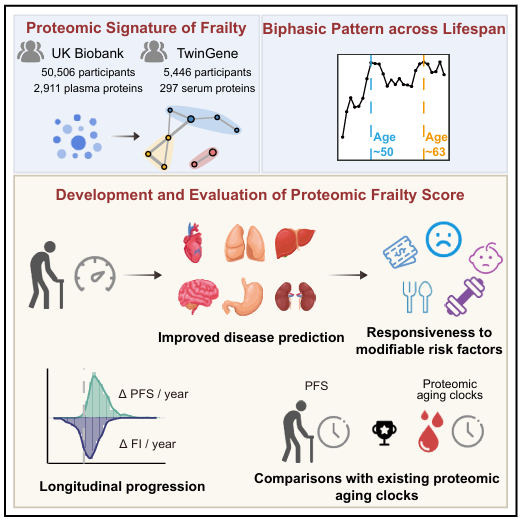
在18个器官系统中,衰弱相关蛋白主要富集于肝脏和胃肠道,心脏、免疫系统、肾脏反而无显著富集。这与直觉不符——人们通常以为衰弱是心脏或免疫问题,但数据指向代谢和消化吸收系统:肝脏管代谢,肠道管营养吸收和免疫调节。
追踪时间:衰弱如何随年龄演变
约1,000名参与者有基线、第三次和第四次访视的蛋白质组数据,为观察衰弱的动态变化提供了条件。
绝大多数参与者的PFS和FI都随时间上升——衰老方向不会变,但速度因人而异。60岁以上人群的PFS年增长率显著高于年轻组,而FI的增长率在各年龄组相对稳定。蛋白质组层面的紊乱在老年阶段加速,临床表型的累积则相对匀速。
PFS每增加一个标准差,平均对应2.5个额外的ICD-10疾病诊断;FI每增加一个标准差对应0.6个。PFS对疾病累积的预测敏感度约是FI的四倍,因为分子层面的变化先于临床诊断出现。
基线衰弱程度越高,PFS增长越快(正相关),但FI增长反而越慢(负相关)。一个可能的解释是临床评估的"天花板效应"——功能缺陷已经很多时,新增项目的空间有限;蛋白质紊乱却可以持续累积。这意味着PFS在重度衰弱人群中仍有动态监测价值。
两个关键转折点:50岁和63岁
研究让人印象深刻的发现之一,是衰弱相关蛋白的变化不是匀速推进,而是呈双峰分布。
在39至71岁年龄段,差异表达蛋白的数量在约50岁和63岁出现两个明显峰值
50岁峰值:富集于胆固醇代谢、脂质分解、碳水化合物衍生物分解、激素活性等代谢通路。中年是代谢稳态开始失调的关键窗口,可能是"代谢型衰弱"的起点。
63岁峰值:富集于白细胞介导免疫、细胞因子-受体互作、抗菌防御等免疫通路,反映老年阶段免疫系统的重塑和炎症状态的加剧,进入"炎症型衰弱"阶段。
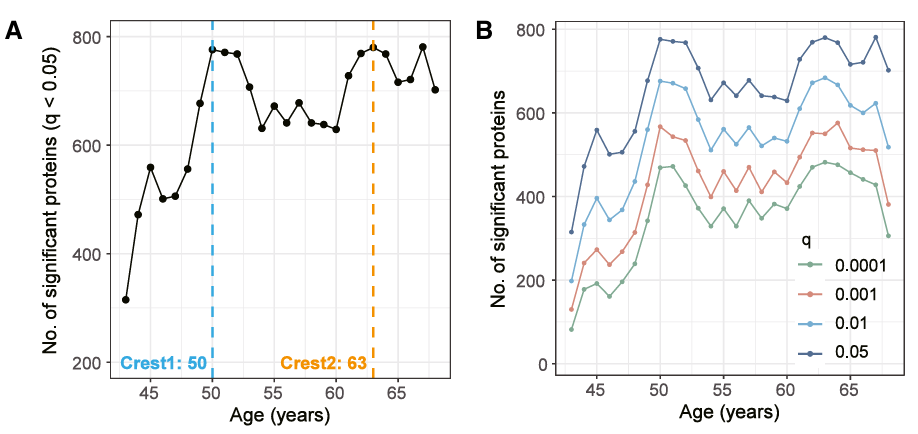
50岁峰值蛋白更多关联代谢指标(总胆固醇、甘油三酯)和帕金森病;63岁峰值蛋白则更多关联多系统疾病(痴呆、心血管疾病、癌症)和炎症标志物。
对公共卫生来说,这个发现的含义很直接:衰弱的预防不是等到老了才开始,50岁左右就该关注代谢;63岁前后则更需要盯住免疫状态和炎症水平。两个阶段的干预重点不同,一刀切没用。
从实验室到生活:这意味着什么
几个值得记住的结论:
第一,衰弱是可以测量的。目前PFS检测还需要研究级平台,但技术迭代不慢。未来几年,体检套餐里出现"衰弱蛋白 panel"不是没有可能。
第二,衰弱是可以干预的。PFS对饮食、运动、戒烟等生活方式因素有响应,这意味着改变习惯可以反映在分子评分上,不只是感觉变好,而是有可量化的指标。
第三,时机比想象中重要。50岁和63岁两个转折点说明,中年的代谢管理和老年的炎症控制是两个不同的干预窗口,不能混为一谈。
第四,老和弱不是同一件事。PFS与通用衰老时钟的差异化表现说明,有人老而不衰,有人未老先衰,这两种轨迹在蛋白质组层面是可以区分的。
写在最后
五万人的血液数据,给出了衰弱的分子轮廓,也给出了人生后半段健康管理的时间坐标。这不是要给人贴标签,而是要在功能下降还可逆的阶段,提供一些有依据的参照。
衰老本身改变不了,但衰弱的速度和程度,很大程度上取决于中间的每一个选择。现在只是有了更好的工具来看清楚这件事。
研究来源:Jia X比较好的证券公司, Gao W, Hagelin H, et al. Plasma proteomic signature of frailty in 50,506 adults. *Cell Metabolism*. 2026;38:1–17.
申宝策略提示:文章来自网络,不代表本站观点。